Untersuchung der Antikörperaggregation und des Molekulargewichts mit dem BeSEC
2026-01-12Application Note
Zusammenfassung: Die Aggregation monoklonaler Antikörper ist ein kritischer Qualitätsfaktor, der die Sicherheit und Wirksamkeit von Biopharmazeutika beeinflusst. In dieser Studie wurde die Größenausschlusschromatographie in Kombination mit statischer Lichtstreuung und Brechungsindexdetektion eingesetzt, um das Molekulargewicht und den Aggregationszustand monoklonaler Antikörper zu charakterisieren und so eine genaue Unterscheidung und Quantifizierung von Monomeren, Dimeren und Aggregaten höherer Ordnung zu ermöglichen.
Schlüsselwörter: Monoklonale Antikörper, Antikörperaggregation, Größenausschlusschromatographie (SEC), Statische Lichtstreuung, Molekulargewichtbestimmung, Biopharmazeutische Charakterisierung
| Produkt | BeSEC |
| Industrie |
Pharmazie, Biologika |
| Probe | Monoklonale Antikörper (Protein) |
| Messmethode | Proteinaggregation und Molekulargewichtsanalyse |
| Mess-Technologie |
Größenausschlusschromatographie (SEC)
|
Einführung
Monoklonale Antikörper (mAbs) sind hochspezifische Proteine, die Antigene auf Krankheitserregern wie Viren und Bakterien erkennen und an diese binden, wodurch eine schnelle Erkennung durch Assays wie ELISA und Immunfluoreszenz ermöglicht wird. Über die Diagnostik hinaus spielen mAbs eine entscheidende Rolle in der Onkologie, indem sie tumorassoziierte Antigene identifizieren und die Krebsfrüherkennung unterstützen. Als Therapeutika können monoklonale Antikörper direkt auf Tumorzellen abzielen; beispielsweise bindet Rituximab an CD20 auf B-Zell-Lymphomzellen und löst so eine immunvermittelte Eliminierung aus. Darüber hinaus können Antikörper mit Chemotherapeutika oder Radionukliden gekoppelt werden, um Antikörper-Wirkstoff-Konjugate (ADCs) zu bilden, die zytotoxische Wirkstoffe an Tumorzellen abgeben und gleichzeitig Nebenwirkungen minimieren.
Bei der Formulierung enthalten monoklonale Antikörperlösungen häufig Dimere, Trimere und Aggregate höherer Ordnung. Diese Spezies können die Immunogenität bei der Verabreichung erhöhen, was Sicherheitsbedenken aufwirft. Daher ist eine genaue Quantifizierung von Oligomeren und Aggregaten für die Formulierungsentwicklung, Qualitätskontrolle und Charakterisierung von Aggregaten unerlässlich.
Experimenteller Abschnitt
Für diese Studie wurde ein Größenausschlusschromatographie-(SEC)-System verwendet, das mit Detektoren für Brechungsindex (RI) und Lichtstreuung (LS) ausgestattet ist. Der LS-Detektor ist das BeSEC LS2 von Bettersize Instruments und ist mit Messwinkeln von 90°- und 7°-ausgestattet. Die BeSEC-Workstation kombiniert Lichtstreuung mit RI- oder UV-Signalen, um Verteilungen sowie Durchschnittswerte des Molekulargewichts (Mn, Mw und Mz) zu berechnen.
Systemkonfiguration:
- Detektoren: Lichtstreuung (LS) + Refraktionsindex (RI)
- Säule: Shodex PROTEIN LW-803
- Mobile Phase: Phosphatgepufferte Kochsalzlösung (PBS)
- Flussrate: 0,7 mL/min
- Injektionsvolumen: 100 μL
- Säulentemperatur: 40 °C
- dn/dc: 0.185 mL/g
Probenvorbereitung:
Drei monoklonale Antikörperproben (A, B und C) wurden für die Analyse vorbereitet. Jede Probe wurde gewogen und in PBS zu einer Konzentration von 2–5 mg/ml gelöst, bis zur vollständigen Transparenz gerührt und anschließend durch einen 0,22-μm-PES-Spritzenfilter filtriert. Die filtrierten Lösungen wurden zur SEC-Injektion in Autosampler-Fläschchen überführt.
Ergebnisse und Diskussion
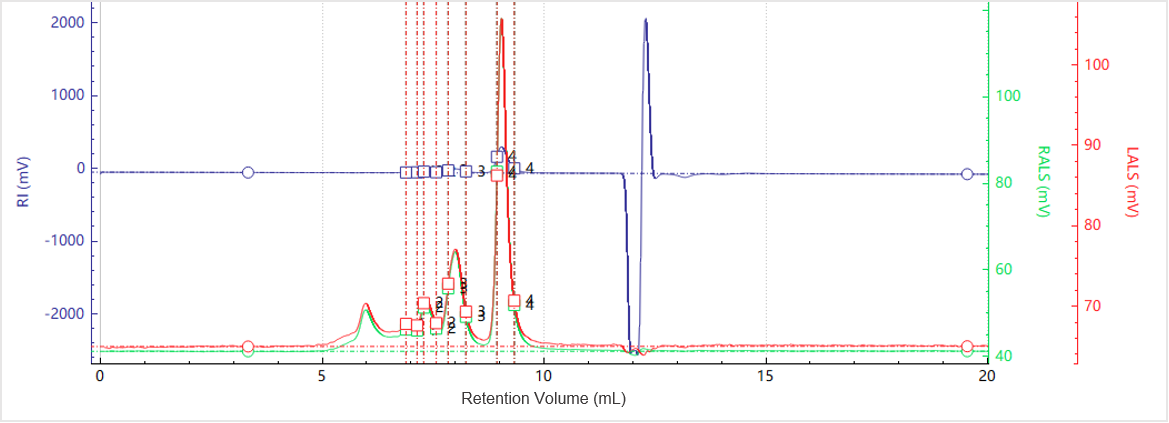
Abbildung 1. Elutionsprofile der Multi-Detektor-Signale für Probe A
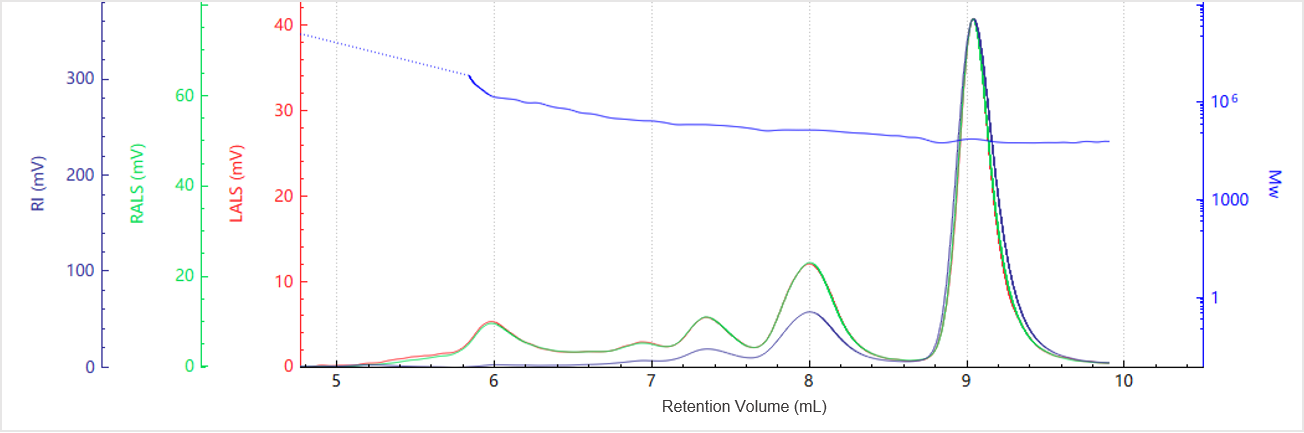
Abbildung 2. Elutionsprofil des Molekulargewichts für Probe A
Abbildung 1 zeigt die Elutionsprofile der Multidetektorsignale für Probe A, während Abbildung 2 die entsprechende Molekulargewichtsverteilung darstellt. Die Lichtstreusignale bei 90° und 7° sowie die RI-Kurve zeigen mehrere deutliche Peaks, was auf das Vorhandensein unterschiedlicher Aggregatzustände innerhalb die Probe hinweist.
Zur Berechnung des Molekulargewichts jeder Spezies wurde die auf den Peaks basierende Integration verwendet, wie in Tabelle 1 zusammengefasst. Das Diagramm „Molekulargewicht gegen Elutionsvolumen” zeigt eine allmähliche Abnahme des Molekulargewichts mit zunehmendem Elutionsvolumen, was mit dem Trennprinzip der SEC übereinstimmt, bei dem größere Spezies früher eluieren als kleinere. Jeder Peak weist ein Molekulargewichtsplateau auf, was die relativ enge Molekulargewichtsverteilung der einzelnen oligomeren Zustände innerhalb der Proteinprobe widerspiegelt.
Tabelle 1. Molekulargewichtsergebnisse für Peaks in Probe A
| Peak | Mw (Da) | Ratio of Peak n/Peak 1 | Area (%) |
| Peak 1 |
149776 |
1 | 75.8 |
| Peak 2 |
295157 |
1.97 | 17.4 |
| Peak 3 |
450351 |
3 | 3.8 |
Das Molekulargewicht von Peak 1 entspricht etwa 150 kDa, was mit dem theoretischen Wert eines monoklonalen Antikörpermonomers übereinstimmt. Die Peaks 2 und 3 skalieren als ganzzahlige Vielfache von Peak 1, was den dimeren und trimeren Spezies entspricht. Die quantitative Analyse zeigt, dass das Monomer 75,80 % des Gesamtproteins ausmacht, während die aggregierten Spezies zusammen mehr als 5 % ausmachen. Bei therapeutischen Anwendungen, die eine Injektion erfordern, sind diese Aggregate bedenklich, da sie das immunogene Risiko erhöhen und die Produktsicherheit beeinträchtigen können.
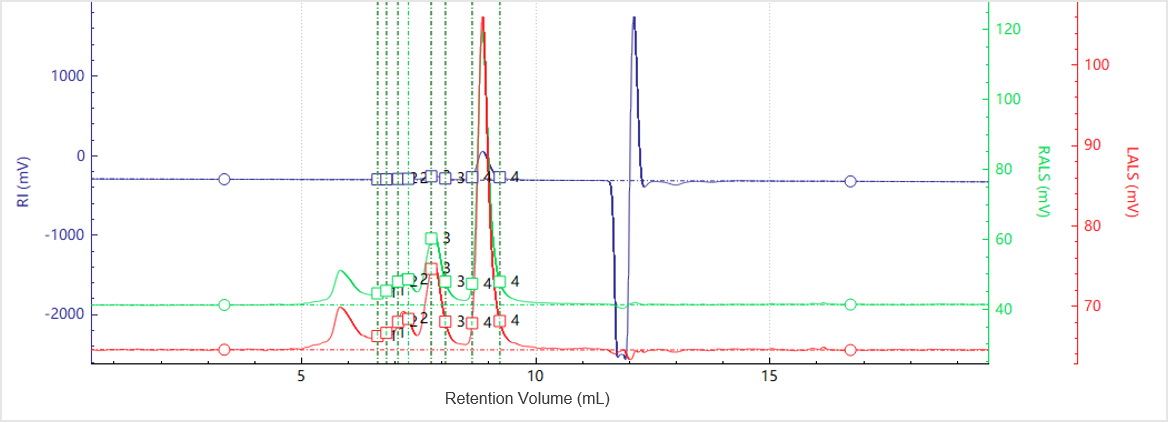
Abbildung 3. Elutionsprofile der Multi-Detektor-Signale für Probe B
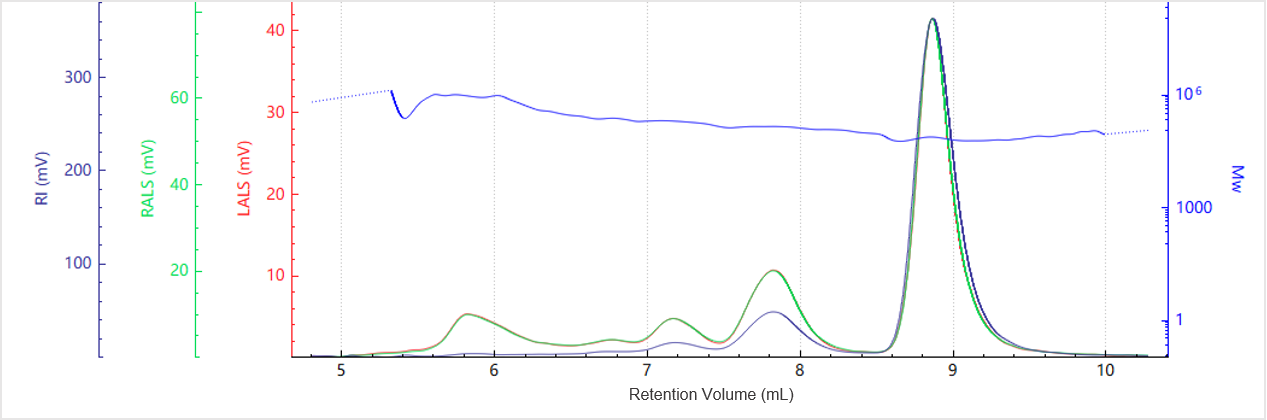
Abbildung 4. Elutionsprofil des Molekulargewichts für Probe B
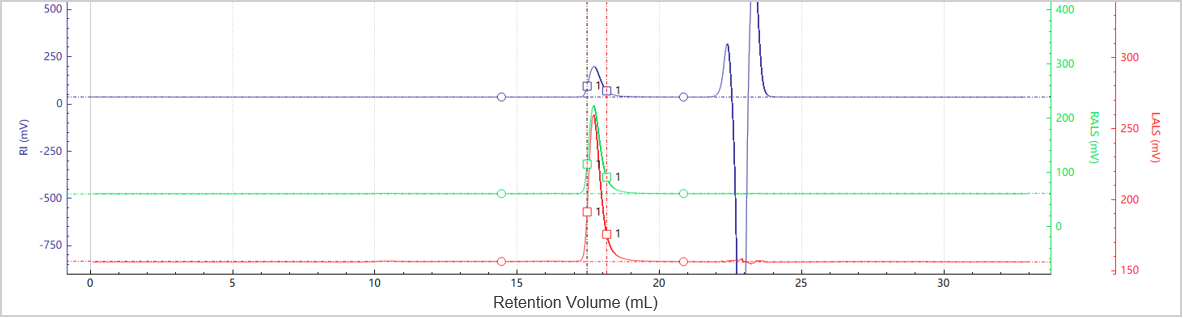
Abbildung 5. Elutionsprofile der Multi-Detektor-Signale für Probe C
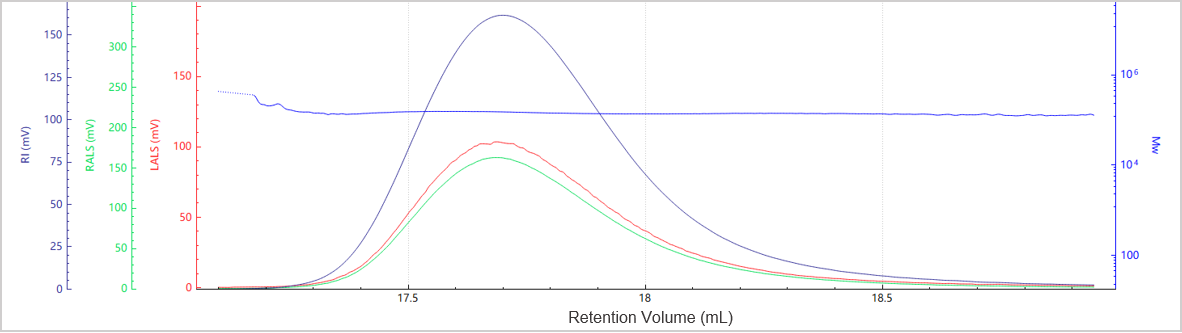
Abbildung 6. Elutionsprofil des Molekulargewichts für Probe C
Die Abbildungen 3 und 4 zeigen das Chromatogramm und das Molekulargewichtsprofil für Probe B. Zusätzlich zum Hauptpeak erscheint ein kleinerer Peak zu einem früheren Elutionszeitpunkt, was auf das Vorhandensein von Aggregaten höherer Ordnung hindeutet.
Die Abbildungen 5 und 6 zeigen das Chromatogramm und das Molekulargewichtsprofil von Probe C, die einen einzigen dominanten Peak aufweist, was darauf hindeutet, dass in dieser Probe nur eine minimale Aggregation vorliegt.
Tabelle 2. Molekulargewichtsergebnisse für Peaks in Probe B
| Peak | Mw (Da) | Ratio of Peak n/Peak 2 | Area (%) |
| Peak 1 |
298048 |
1.97 | 1.34 |
| Peak 2 |
151546 |
1 | 98.6 |
Tabelle 3. Molekulargewichtsergebnisse für Peaks in Probe C
| Peak | Mw (Da) | Ratio of Peak n/Peak 2 | Area (%) |
| Peak 1 |
147709 |
1 | 100 |
Tabelle 2 zeigt, dass Probe B zusätzlich zum primären Monomerpeak ein Dimer enthält. Das Molekulargewicht des Dimers ist etwa doppelt so hoch wie das des Monomers, und seine relative Häufigkeit ist mit 1,34 % gering, was auf eine minimale Aggregation hindeutet. Im Gegensatz dazu zeigt Tabelle 3, dass Probe C ausschließlich den Hauptpeak enthält, ohne dass Oligomere oder Aggregate höherer Ordnung nachweisbar sind. Dieses Profil spiegelt eine ausgezeichnete strukturelle Integrität wider und deutet darauf hin, dass Probe C die stabilste der drei getesteten Formulierungen ist.
Schlussfolgerung
In dieser Anwendungsbeschreibung wurde der BeSEC LS2-Detektor zur Messung der Molekulargewichte von monoklonalen Antikörperproben eingesetzt. Aggregate in Biopharmazeutika können die therapeutische Wirksamkeit und die Patientensicherheit erheblich beeinträchtigen, da große Aggregate Immunreaktionen auslösen können. Daher ist es von entscheidender Bedeutung, die Art und den Gehalt an Aggregaten in monoklonalen Antikörperformulierungen zu kennen. Das BeSEC-System zeigt, dass statische Lichtstreuung Monomere, Dimere und höherwertige Spezies effektiv auflösen und deren Gehalt quantifizieren kann. Diese Möglichkeit ist für die Entwicklung, Stabilitätsbewertung und Qualitätssicherung von biologischen Arzneimitteln von großem Wert.
About the Authors
 |
Zhibin Guo |
|
BeSEC
Advanced Light Scattering Detector
|
LOGIN TO ACCESS EXCLUSIVE CONTENT
More Resources Including
- Application Notes & Collections
- Webinars & Workshops
- Presentations & Videos
- Monthly Newsletters
- Exclusive Events...

Recommended articles
Rate this article
