Значение гранулометрического анализа для API
2020-09-17Application Briefs
Качество и контроль лекарств
Качество лекарств зависит от множества параметров. Скорость растворения препарата в организме человека является одним из основных показателей качества лекарств и контроля над ними. Под скоростью растворения понимается скорость всасывания препарата в ткани и органы. При приготовлении твердых лекарственных препаратов лекарство, поглощаемое человеческим организмом, должно пройти процесс дезинтеграции и растворения. Если лекарство не может легко высвобождаться из организма или скорость его растворения крайне низкая, возникнут проблемы с приемом этого конкретного препарата. С другой стороны, некоторые препараты обладают слишком быстрым фармакологическим действием, что может сделать их небезопасными. Если лекарство растворяется слишком быстро, это может резко сократить время его действия в организме человека, но не только это может вызвать значительные побочные реакции. В этом случае подготовка к контролю скорости растворения лекарств особенно важна. Степень растворения препарата в растворителе выражается скоростью растворения. Таблетка - это распространенная лекарственная форма для перорального приема, и скорость растворения тесно связана с гранулометрическим составом сырья и вспомогательных веществ, рецептурным составом, твердостью частиц и условиями обработки. При производстве активного фармацевтического ингредиента (API) размер частиц является обязательным параметром. В зависимости от требований, предъявляемых к растворению различных таблеток, размер частиц АФИ должен контролироваться в различных гранулометрических сегментах для достижения максимальной эффективности.
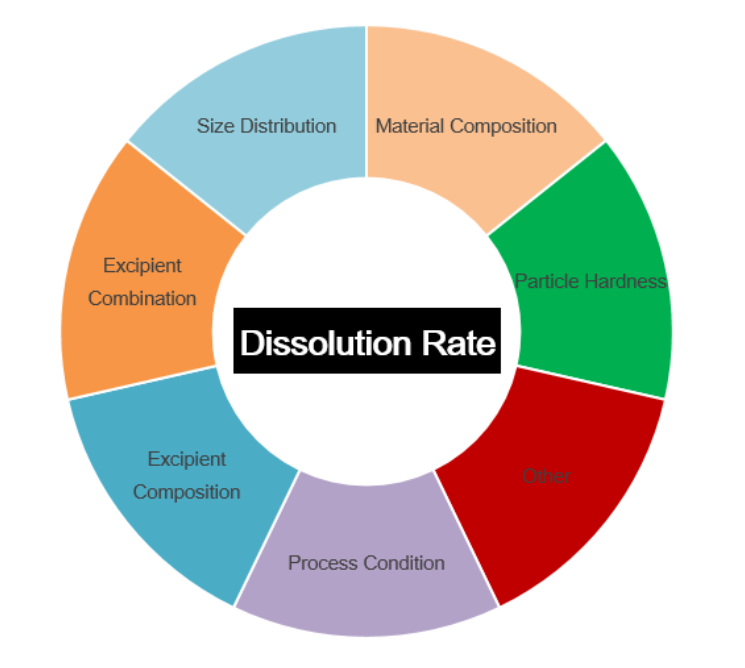
Рисунок 1. Взаимосвязь между свойствами лекарственных препаратов и скоростью растворения
Скорость растворения
Скорость растворения является ключевым параметром оценки для научно-исследовательских учреждений, занимающихся разработкой лекарственных препаратов, для оптимизации процесса создания рецептуры таблеток, а также для контролирующих органов, которые следят за качеством и эффективностью таблеток. Она является основным методом прогнозирования биодоступности и биоэквивалентности лекарственных средств. По мнению Международного координационного комитета Китая и многих других стран мира в отношении важнейших технических требований к регистрации лекарственных средств для человека, процесс приготовления стал центром внимания и спроса для фармацевтических исследовательских учреждений. Независимо от того, идет ли речь о разработке генерических или патентованных препаратов, они не могут отступать от оценки последовательности, исследования растворения лекарств необходимы сейчас и в нашей жизни для будущего.
Помимо таблеток, при ингаляционном приготовлении размер частиц API напрямую влияет на равномерность дозы и эффективность осаждения в легких. Слишком крупные частицы попадают в горло и не доходят до легких, а слишком мелкие попадают в легкие и не задерживаются там, а выдыхаются в атмосферу. Оптимальный размер частиц составляет от 1 до 7 микрон. В препаратах для внутривенного введения крупные нерастворимые частицы напрямую влияют на безопасность состава. Фармацевтический эксципиент, размер частиц, морфология и ликвидность напрямую влияют на формуемость, однородность и дезинтеграцию, растворение, твердость таблетки и внешний вид препарата. Поэтому мировые фармакопеи рассматривают обнаружение и оценку частиц лекарственного средства как очень важный параметр свойств.
Лазерно-дифракционный анализ распределения частиц по размерам в фамотидине
Фамотидин используется во многих лекарственных формах, включая таблетки, капсулы и инъекционные препараты. Фамотидин является антагонистом гистаминовых H2-рецепторов, который может подавлять секрецию желудочной кислоты. Он подходит для лечения язвы желудка и двенадцатиперстной кишки, рефлюкс-эзофагита, кровотечений в верхних отделах желудочно-кишечного тракта, синдрома Золлингера-Эллисона и других заболеваний. Измерение гранулометрического состава сырья и вспомогательных веществ для этого препарата с помощью лазерной дифракции было внесено в фармакопеи многих стран. Распределение частиц по размерам рассчитывается методом лазерной дифракции, при котором теоретическая модель Ми рассчитывает распределение частиц по размерам на основе интенсивности света, получаемого каждым детектором после его обесцвечивания. Здесь мы видим распределение частиц по размерам, полученное в результате лазерного дифракционного анализа фамотидина.
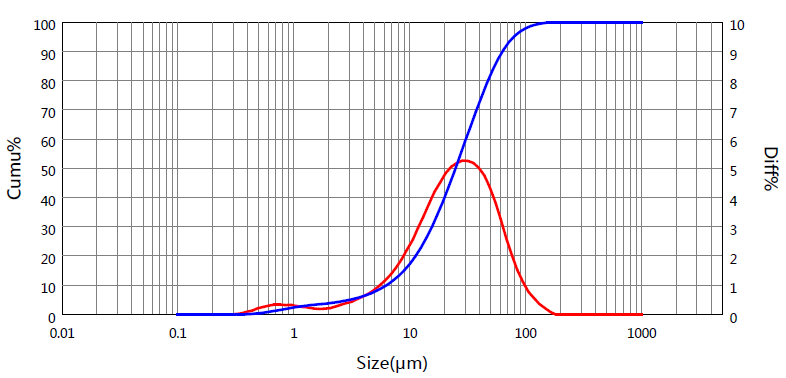
Рисунок 2. Диаграмма распределения частиц по размерам для одного образца фамотидина
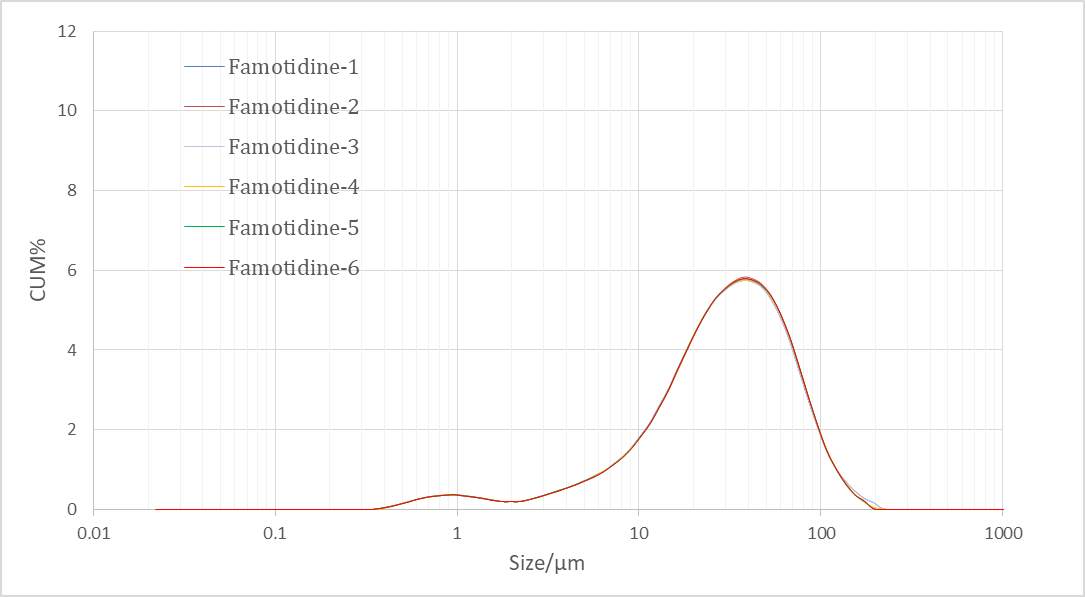
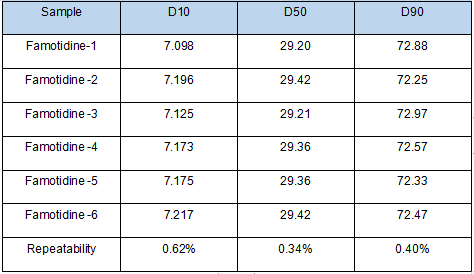
Рисунок 3. Анализ размера частиц образцов фамотидина с помощью прибора Bettersizer 2600
Анализ изображений фамотидина


Рисунок 5. Анализ изображения Фамотидина-2 в измерении BeVision S1
При анализе изображений можно непосредственно наблюдать морфологию и структуру частиц и создавать математические модели и сложные алгоритмы. Компания Bettersize сделала технологию измерения простой и интуитивно понятной, чтобы каждый пользователь мог стать экспертом.
По наблюдениям в микроскоп, эффект дисперсии двух образцов хороший, и нет явления агломерации. Частицы почти все игольчатые, полупрозрачные, а крупные частицы составляют от 100 до 200 мм, что соответствует данным, измеренным лазерным анализатором размера частиц.
Заключение
Лазерная дифракция - мощная технология, широко используемая для определения размера частиц сырья и вспомогательных материалов. Преимуществами этого метода являются высокая скорость определения и высокая точность. Однако у технологии лазерной дифракции есть и непреодолимые недостатки. Технология лазерной дифракции не может напрямую определить размер и форму активного фармацевтического ингредиента в целой капсуле или таблетке. Лазерная дифракция может показать только распределение по размерам всего ингредиента препарата, как в случае с фамотидином. Поэтому использование анализа изображений для перекрестной валидации очень необходимо. С помощью системы анализа изображений можно интуитивно определить размер конечных частиц, при этом невозможно определить, является ли образец агломерированным или разрушенным. Кроме того, для многих препаратов очень важна форма кристаллов основного и вспомогательных веществ. Сочетание этих двух методов позволяет не только получить распределение размеров для исследования скорости растворения на основе лазерной дифракции, но и может иметь большое значение для оптимизации процесса создания формулы препарата на основе анализа изображений. Качество лекарств нелегко контролировать, но Bettersize всегда может дать отличное решение в частицах для фармацевтических исследований и разработок.
LOGIN TO ACCESS EXCLUSIVE CONTENT
More Resources Including
- Application Notes & Collections
- Webinars & Workshops
- Presentations & Videos
- Monthly Newsletters
- Exclusive Events...



